ņä£ļĪĀ
ņŗĀĻ▓Į ņĪ░ņ¦üņØś ĻĄ¼ņĪ░ļź╝ ņŚ░ĻĄ¼ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ļÅÖļ¼╝ņØä ņé¼ņÜ®ĒĢśļŖö ņŗżĒŚśņĀü ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒØöĒ׳ Ļ┤æĒĢÖĒśäļ»ĖĻ▓ĮņØ┤ļéś ņĀäņ×ÉĒśäļ»ĖĻ▓ĮņØä ņØ┤ņÜ®ĒĢ£ļŗż. ĻĘĖļ¤¼ļéś ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ļÅä ĻĄ¼ņĪ░ņØś ņŚ░ĻĄ¼Ļ░Ć Ļ░ĆļŖźĒĢśļŗżļŖö Ļ▓āņØä Kim ļō▒ņØ┤[
1] ļ│┤Ļ│ĀĒĢ£ ļ░öĻ░Ć ņ׳ļŗż.
X-ņäĀ ņé░ļ×Ć ĻĖ░ļ▓ĢņØĆ ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░ļź╝ ņØ┤ņÜ®ĒĢ£ ĻĄ¼ņĪ░ļČäņäØļ▓ĢņØś ĒĢśļéśļĪ£ ĻĘĖ ņżæ ņåīĻ░ü X-ņäĀ ņé░ļ×Ć(small-angle X-ray scattering, SAXS)ĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŗĀĻ▓Į ĻĄ¼ņĪ░ņØś ļ│ĆĒÖöļź╝ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŗż[
2,
3].
Ļ┤æĒĢÖĒśäļ»ĖĻ▓ĮņØ┤ļéś ņĀäņ×ÉĒśäļ»ĖĻ▓ĮņØä ņé¼ņÜ®ĒĢśņŚ¼ ņŚ░ĻĄ¼ĒĢśļŖö Ļ▓ĮņÜ░ņŚÉļŖö ņĪ░ņ¦üņØś Ļ│ĀņĀĢ, ņĀłĒÄĖ ĻĘĖļ”¼Ļ│Ā ĒÖöĒĢÖņĀü ņ▓śļ”¼ ļō▒Ļ│╝ Ļ░ÖņØĆ Ļ│╝ņĀĢņØ┤ ĒĢäņÜöĒĢśļ®░ ņ▓śļ”¼Ļ│╝ņĀĢņØä ņ£äĒĢ£ ņŗ£Ļ░ä ļśÉĒĢ£ ņÜöĻĄ¼ļÉ£ļŗż. ĒŖ╣Ē׳ ņŗĀĻ▓ĮņĪ░ņ¦üņØĆ ĒÖöĒĢÖņĀü ņ▓śļ”¼Ļ│╝ņĀĢņ£╝ļĪ£ ņØĖĒĢ┤ ņŗ£ļŻīņØś ņåÉņāüĻ│╝ artifactĻ░Ć ļ░£ņāØĒĢĀ ņłśĻ░Ć ņ׳ļŗż[
4,
5]. ļśÉĒĢ£ Ļ┤æĒĢÖĒśäļ»ĖĻ▓ĮņØ┤ļéś ņĀäņ×ÉĒśäļ»ĖĻ▓ĮņØä ņØ┤ņÜ®ĒĢśļŖö Ļ▓ĮņÜ░ņŚÉļŖö ņĪ░ņ¦üņØś ņĀłĒÄĖņ£╝ļĪ£ ņŚ░ĻĄ¼ĒĢśĻ▓ī ļÉ£ļŗż. ņØ┤ņŚÉ ļ╣äĒĢ┤ SAXS ĻĖ░ļ▓Ģņ£╝ļĪ£ ņŗ£Ē¢ēĒĢĀ ņŗ£ņŚÉļŖö ņĪ░ņ¦ü ņŻ╝ņ£äĻ░Ć ņלļ”░ Ļ▓āņØä ņĀ£ņÖĖĒĢśĻ│ĀļŖö ņĪ░ņ¦üņØś ņ▓śļ”¼ļź╝ ĒĢśņ¦Ć ņĢŖņØĆ ņøÉņāüĒā£ļĪ£ ņŚ░ĻĄ¼ĒĢśļŖöļŹ░ ļ¦żņÜ░ ņ£ĀņÜ®ĒĢśļ®░[
2,
3], ņĖĪņĀĢņŗ£Ļ░äņØ┤ ļ¦żņÜ░ ņ¦¦ņĢäņä£(60ņ┤ł ņØ┤ļé┤) ļ│Ćņä▒ļÉśņ¦Ć ņĢŖņØĆ ņāüĒā£ņØś ļéśļģĖ ĻĄ¼ņĪ░ ņĀĢļ│┤ļź╝ ņĀĢĒÖĢĒ׳ ņĀ£Ļ│ĄĒĢĀ ņłś ņ׳ņ¢┤ ļ░öņØ┤ņśż ļ¼╝ņ¦łņØś ĻĄ¼ņĪ░ņŚ░ĻĄ¼ņŚÉ ļ¦żņÜ░ ņĀüĒĢ®ĒĢśļŗż.
ĻĘĖļ¤¼ļéś ņØ┤ļ¤¼ĒĢ£ ņןņĀÉņØ┤ ņ׳ņØīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░Ļ░Ć ĻĄŁļé┤ņŚÉņä£ ĒżĒĢŁ ĒĢ£Ļ││ņŚÉļ¦ī ņ׳ĻĖ░ņŚÉ ņØ┤ļź╝ ņØ┤ņÜ®ĒĢĀ ņŗ£ņŚÉļŖö ņŗ£Ļ░äņØś ņĀ£ĒĢ£ņØ┤ ņ׳ļŗż. ļśÉĒĢ£ ņĢäņ¦ü ļÅÖļ¼╝ņŗżĒŚśņŗżņØ┤ ņżĆļ╣ä ņżæņŚÉ ņ׳ĻĖ░ņŚÉ ļÅÖļ¼╝ņØä in vivo Ēś╣ņØĆ ex vivo ņāüĒā£ņŚÉņä£ ņŚ░ĻĄ¼ļź╝ ņŗ£Ē¢ēĒĢśļĀżļ®┤ ļ»Ėļ”¼ ņØ┤ņÜ®ņŗ£Ļ░äņŚÉ ļ¦×ņČöņ¢┤ ņŗżĒŚśņĪ░Ļ▒┤ņØä ļ¦īļōżņ¢┤ņĢ╝ ĒĢśĻ│Ā ņ¦üņĀæ ņżĆļ╣äĒĢ£ ļÅÖļ¼╝ņØä Ļ░ĆņĀĖĻ░ĆņĢ╝ ĒĢśĻ│Ā, ņĪ░ņ¦üņĀüņČ£ņØä ĻĘĖĻ││ņŚÉņä£ ĒĢ┤ņĢ╝ĒĢśļŖö ļō▒ ņŗżĒŚśĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ņĀ£ĒĢ£ņĀÉņØ┤ ņ׳ļŗż.
ņØ┤ņŚÉ ļ│Ė ņŚ░ĻĄ¼ļŖö ņØ┤ļ¤¼ĒĢ£ ņĀ£ĒĢ£ņĀÉņØä ļ│┤ņÖäĒĢśņŚ¼ Ļ░ĆņåŹĻĖ░ ņÜ┤ņÜ®ņŗ£Ļ░äņŚÉ ņŗżĒŚśĒĢĀ ņłś ņ׳ļÅäļĪØ ņźÉ ĻČüļæźņŗĀĻ▓ĮņØä ļ»Ėļ”¼ ņĀüņČ£ĒĢ£ Ēøä Ēżļź┤ļ¦Éļ”░, ņĢĪĒÖöņ¦łņåī, ĻĘĖļ”¼Ļ│Ā ņāØļ”¼ņŗØņŚ╝ņłśļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ļ│┤Ļ┤ĆĒĢśļŖö ļ░®ļ▓ĢņØ┤ SAXS ĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢ ņŗ£ ņØ┤ņØś Ļ▓░Ļ│╝ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØ┤ ņ׳ļŖöĻ░Ćļź╝ ņĪ░ņé¼ĒĢśĻ│Āņ×É ņŗ£Ē¢ēĒĢśņśĆļŗż.
ļīĆņāü ļ░Å ļ░®ļ▓Ģ
ļ│Ė ņŚ░ĻĄ¼ļŖö ļ│Ė ņØśļŻīņøÉ ļÅÖļ¼╝ ņ£żļ”¼ņ£äņøÉĒÜīņØś ņŖ╣ņØĖ ĒĢśņŚÉ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░(2010-1222-CU-AEC-8-Y) ņŗżĒŚśļÅÖļ¼╝ļōżņØĆ ļ│Ė ļ│æņøÉņØś IACUC (Institutional animal care and use committee)ņŚÉ ĻĖ░ņłĀļÉ£ Ļ░ĆņØ┤ļō£ļØ╝ņØĖņŚÉ ļö░ļØ╝ Ļ┤Ćļ”¼ĒĢśņśĆļŗż.
ņŗżĒŚśļÅÖļ¼╝ļĪ£ ņŚ░ļĀ╣ņØ┤ 7ņŻ╝(ņ▓┤ņżæ 250-350 gram)ņØĖ ņøģņä▒ ļ░▒ņä£(Sprague-Dawly rat)ļź╝ ļīĆņāüņ£╝ļĪ£ ĒĢśņśĆņ£╝ļ®░ ņŗżĒŚś ņĀä 1-2ņØ╝Ļ░ä ļÅÖļ¼╝ ņé¼ņ£Ī ņŗżņŚÉņä£ ņĢłņĀĢĒåĀļĪØ ĒĢśņśĆļŗż.
ņŗżĒŚś ĻĄ░ņØĆ ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░ļź╝ ņØ┤ņÜ®ĒĢśĻĖ░ļĪ£ ļ░░ņĀĢ ļ░øņØĆ ļéĀ ĒĢśļŻ© ņĀäņŚÉ ĻČüļæźņŗĀĻ▓ĮņØä ņĀüņČ£ĒĢ£ Ēøä ņāØļ”¼ņŗØņŚ╝ņłś(N = 2), Ēżļź┤ļ¦Éļ”░ ņÜ®ņĢĪ(ņĢīļŹ░ĒĢśņØ┤ļō£Ļ│äņŚ┤ [0.1% Glutaaldehyde + 4% Paraformaldehyde, PFA]) (N = 2), ĻĘĖļ”¼Ļ│Ā ņĢĪĒÖöņ¦łņåī(liquid nitrogen, N = 2)ņŚÉ ĒĢśļŻ© ļÅÖņĢł ļ│┤ņĪ┤ĒĢ£ ĻĄ░ņ£╝ļĪ£ ĒĢśņśĆļŗż. ņĢĪĒÖöņ¦łņåīņŚÉ ļ│┤Ļ┤ĆĒĢ£ ĻĄ░ņØĆ ņŗżĒŚś ņ¦üņĀäņŚÉ ņŗżņś©ņŚÉņä£ ļģ╣ņØĖ Ēøä ņŗżĒŚśĒĢśņśĆļŗż. ļīĆņĪ░ĻĄ░(N = 3)ņØĆ ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŗżĒŚśņØä ĒĢśĻĖ░ ņ¦üņĀäņŚÉ ĻČüļæźņŗĀĻ▓ĮņØä ņĀüņČ£ĒĢ£ ĻĄ░ņ£╝ļĪ£ ĒĢśņśĆļŗż. ļæÉ ĻĄ░ ļ¬©ļæÉ ĻČüļæźņŗĀĻ▓ĮņŚÉ ņĢäļ¼┤ļ¤░ ņĪ░ņ×æņØä ĒĢśņ¦Ć ņĢŖņĢśļŗż. ļ¦łņĘ©ļŖö ļæÉ ĻĄ░ ļ¬©ļæÉņŚÉņä£ ņ╝ĆĒāĆļ»╝ 80 mg/kgņØä ļ│ĄĻ░Ģ ļé┤ļĪ£ ņŻ╝ņ×ģĒĢśņŚ¼ ņŗ£Ē¢ēĒĢśņśĆĻ│Ā Ļ╝¼ļ”¼ļ╝łņŚÉ ņ×ÉĻĘ╣ņØä ņŻ╝ņ¢┤ ņøĆņ¦üņØ┤ņ¦Ć ņĢŖņØä ņŗ£ ļ¦łņĘ©Ļ░Ć ļÉśņŚłļŗżĻ│Ā ĒīÉļŗ©ĒĢśņśĆļŗż. Ēś╣ ņøĆņ¦üņ×äņØ┤ ņ׳ņØä ņŗ£ ļ│ĄĻ░Ģ ļé┤ļĪ£ ņČöĻ░Ć ņŻ╝ņ×ģĒĢ£ Ēøä ņŗ£Ē¢ēĒĢśņśĆļŗż.
ņĀüņČ£ĒĢ£ ļäż ĻĄ░ņØś ĻČüļæźņŗĀĻ▓ĮņØĆ ĒÅ┤ļ”¼ņØ┤ļ»Ėļō£ ĒĢäļ”ä ņé¼ņØ┤ņŚÉ ļü╝ņøī ļäŻņØĆ Ēøä ņל ļ░Ćļ┤ēĒĢśņŚ¼ ņĖĪņĀĢĒĢśļŖö ļÅÖņĢł ņłśļČäņØś ņ”Øļ░£ņŚÉ ņØśĒĢ£ ļ│ĆĒśĢņØä ļ░®ņ¦ĆĒĢśņśĆļŗż.
ņåīĻ░ü X-ņäĀ ņé░ļ×Ć(small angle X-ray scattering, SAXS) ļ▓ĢņØś ņŗżĒŚśņØĆ ĒżĒĢŁ ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░ ņŚ░ĻĄ¼ņåīņØś 4C1 SAXS ļ╣ö ļØ╝ņØĖņŚÉņä£ ņłśĒ¢ēĒĢśņśĆļŗż. ņé¼ņÜ®ļÉ£ X-ņäĀņØś ņŚÉļäłņ¦ĆļŖö 11 keVņØ┤ņŚłņ£╝ļ®░, ņŗ£ļŻīņŚÉņä£ X-ņäĀ Ļ▓ĆņČ£ĻĖ░Ļ╣īņ¦ĆņØś Ļ▒░ļ”¼ļŖö 3 mļĪ£ ņØ┤ļĢī ņĖĪņĀĢ Ļ░ĆļŖźĒĢ£ ņĄ£ļīĆ ļ®┤Ļ░äĻ▒░ļ”¼(dmax)ļŖö ņĢĮ 150 nmņØ┤ņśĆļŗż. X-ņäĀ Ļ▓ĆņČ£ĻĖ░ļĪ£ļŖö ņ¦Ćļ”ä 165 mmņØĖ 2ņ░©ņøÉ Ļ▓ĆņČ£ĻĖ░(MarCCD, Mar USA, Inc. Evanston, IL, USA)ļź╝ ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░ SAXS Ēī©Ēä┤ņØä ņĖĪņĀĢĒĢśĻĖ░ ņ£äĒĢ£ ļģĖņČ£ņŗ£Ļ░äņØĆ Ļ░üĻ░ü 60ņ┤łņśĆļŗż.
ņĖĪņĀĢņŚÉ ņé¼ņÜ®ļÉ£ ĻČüļæźņŗĀĻ▓ĮņØś ĻĖĖņØ┤ļŖö Ļ░üĻ░ü ņĢĮ 15 mmņØ┤ņśĆņ£╝ļ®░ ņĖĪņĀĢ ņŗ£ ņŗĀĻ▓ĮņØä ņłśņ¦üņ£╝ļĪ£ Ļ▒░ņ╣śĒĢ£ Ēøä ņłśĒÅēļ░®Ē¢źĻ│╝ ņłśņ¦üļ░®Ē¢źņ£╝ļĪ£ ņłśņ┤ł, ņä¼ņ£ĀņåīĻ░äņØś Ļ▒░ļ”¼ņÖĆ ņĮ£ļØ╝ņĀĀ ņä¼ņ£Āļź╝ ņĖĪņĀĢĒĢśņśĆļŗż. SAXS Ēī©Ēä┤ņØĆ Ļ░üĻ░üņØś ĻČüļæźņŗĀĻ▓ĮņØä ĻĖĖņØ┤ ļ░®Ē¢źņ£╝ļĪ£ 0.5 mmĻ░äĻ▓®ņ£╝ļĪ£ 8-12Ļ││ņŚÉ ņĖĪņĀĢĒĢśņśĆļŗż.
Ļ▓░Ļ│╝
ļ│┤ņĪ┤ ņ▓śļ”¼ĒĢśņ¦Ć ņĢŖņØĆ ņźÉ ĻČüļæźņŗĀĻ▓ĮņØś SAXS Ēī©Ēä┤
ņåīĻ░ü X-ņäĀ ņé░ļ×Ćļ▓Ģņ£╝ļĪ£ ņĖĪņĀĢĒĢśĻĖ░ ņ¦üņĀäņŚÉ ņĀüņČ£ĒĢ£ ņĀĢņāü ņźÉ ĻČüļæźņŗĀĻ▓ĮņØä ņłśņ¦üļ░®Ē¢źņ£╝ļĪ£ ņ£äņ╣śņŗ£Ēé© Ēøä SAXS ĒÜīņĀł Ēī©Ēä┤ņØä ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ ņłśņ¦üļ░®Ē¢źĻ│╝ ņłśĒÅēļ░®Ē¢źņŚÉņä£ Ļ░üĻĖ░ ļŗżļźĖ ņŻ╝ĻĖ░ņä▒ņØä Ļ░Ćņ¦ĆļŖö ĒÜīņĀłĒī©Ēä┤ņØä ļ│┤ņśĆļŗż. ņłśĒÅēļ░®Ē¢źĻ│╝ ņłśņ¦üļ░®Ē¢źņ£╝ļĪ£ ņĖĪņĀĢļÉ£ ņØ╝ņ░©ņøÉņĀüņØĖ(1 dimension, ID) ņåīĻ░ü ĒÜīņĀł ļŹ░ņØ┤ĒāĆļź╝
Fig. 1AņÖĆ
Fig. 2AņŚÉ ļéśĒāĆļāłļŖöļŹ░
Fig. 1AļŖö ņłśĒÅē ļ░®Ē¢źņ£╝ļĪ£ņØś 1D ņåīĻ░ü ĒÜīņĀł ļŹ░ņØ┤Ēä░ļź╝ ļéśĒāĆļéĖ Ļ▓āņ£╝ļĪ£ ņĢĮ 18 nm ņČĢ ņŻ╝ĻĖ░ņä▒(axial periodicity)ņØä ļéśĒāĆļé┤ļŖö ņłśņ┤ł(myelin sheath)ņØś ĒÜīņĀł Ēö╝Ēü¼ļōż(M
1st, M
2nd ĻĘĖļ”¼Ļ│Ā M
3rd)Ļ│╝ ņĢĮ 66 nmņØś ņČĢ ņŻ╝ĻĖ░ņä▒ņØä ļéśĒāĆļé┤ļŖö ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåīļōż ņé¼ņØ┤ņØś Ļ▒░ļ”¼(interfibrillar distance)ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö ĒÜīņĀłĒö╝Ēü¼(F
1st, F
2nd)Ļ░Ć ņĖĪņĀĢļÉśņŚłļŗż. ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåīļōż ņé¼ņØ┤ņØś Ļ▒░ļ”¼ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö ĒÜīņĀłĒö╝Ēü¼ļŖö ĒÅŁņØ┤ ņāüļŗ╣Ē׳ ļäōĻ│Ā ļśÉĒĢ£ ĒÜīņĀł ņäĖĻĖ░ļÅä ļ¦żņÜ░ ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż.
Fig. 2A ļŖö ņłśņ¦ü ļ░®Ē¢źņ£╝ļĪ£ņØś 1D ņåīĻ░ü ĒÜīņĀł ļŹ░ņØ┤Ēä░ļź╝ ļéśĒāĆļéĖ Ļ▓āņ£╝ļĪ£ ņĢĮ 67 nmņØś ņČĢ ņŻ╝ĻĖ░ņä▒ņØä ļéśĒāĆļé┤ļŖö ņĮ£ļØ╝Ļ▓ÉņØś ĒÜīņĀł peak ļōż(C
1st-C
9th)ņØ┤ ļÜ£ļĀĘĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż.
Fig.┬Ā1
One dimensional SAXS plot of nerve in ex vivo state (normal) and nerve preserved for one day in formalin, normal saline and liquid nitrogen (LN2) measured by using of SAXS at horizontal direction. Myelin sheath was measured as 18 nm periodicity peak patterns (M1st, M2nd, M3rd,) in ex vivo state (A). Interfibrillar distance was between collagen fibrils measured 66 nm periodicity peak patterns (F1st, F2nd) which is wide and weak in ex vivo state (A). Periodic peaks, F1st and F2nd, of nerve preserved in formalin and saline were not measured (B, C). The Measured periodic peaks and intensity, M1, M2 and M3, of nerve preserved in formalin and saline were weak and/or not detected. Periodic peaks and intensity, F1st, F2nd and M1, M2, M3, of nerve preserved in liquid nitrogen, were comparable to those of nerve in ex vivo state (D).
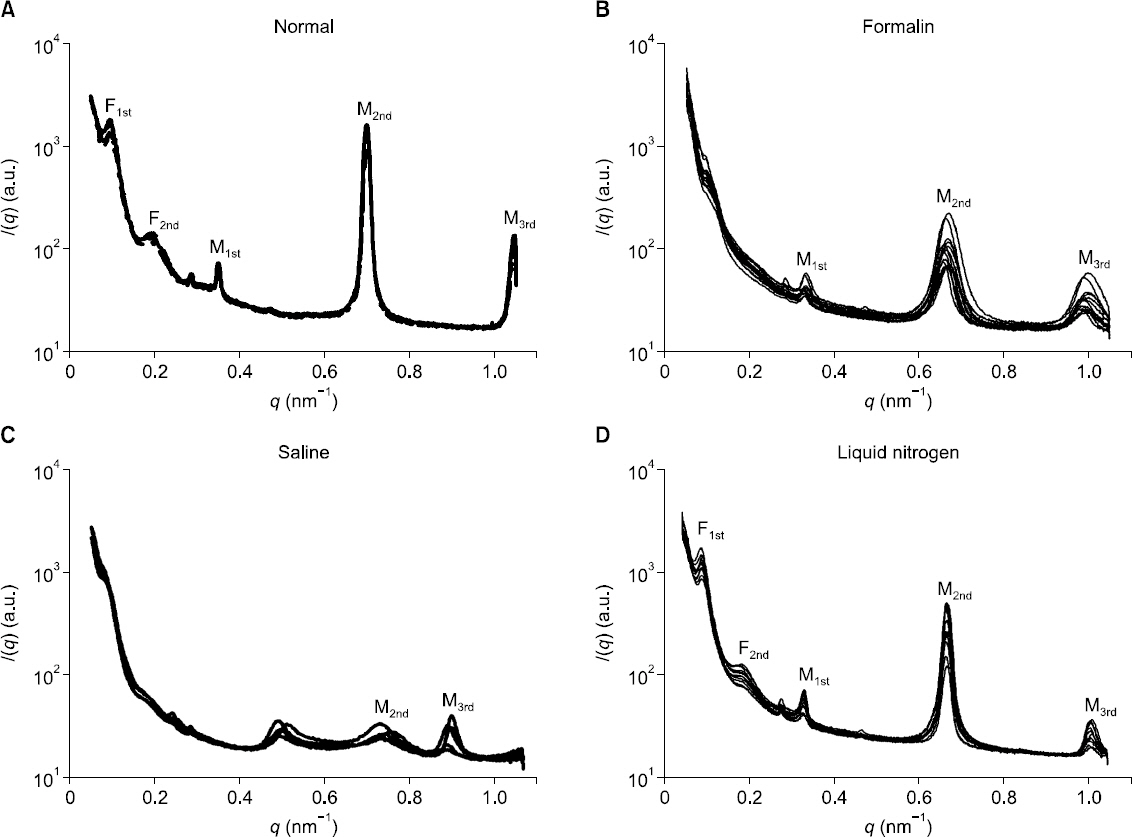
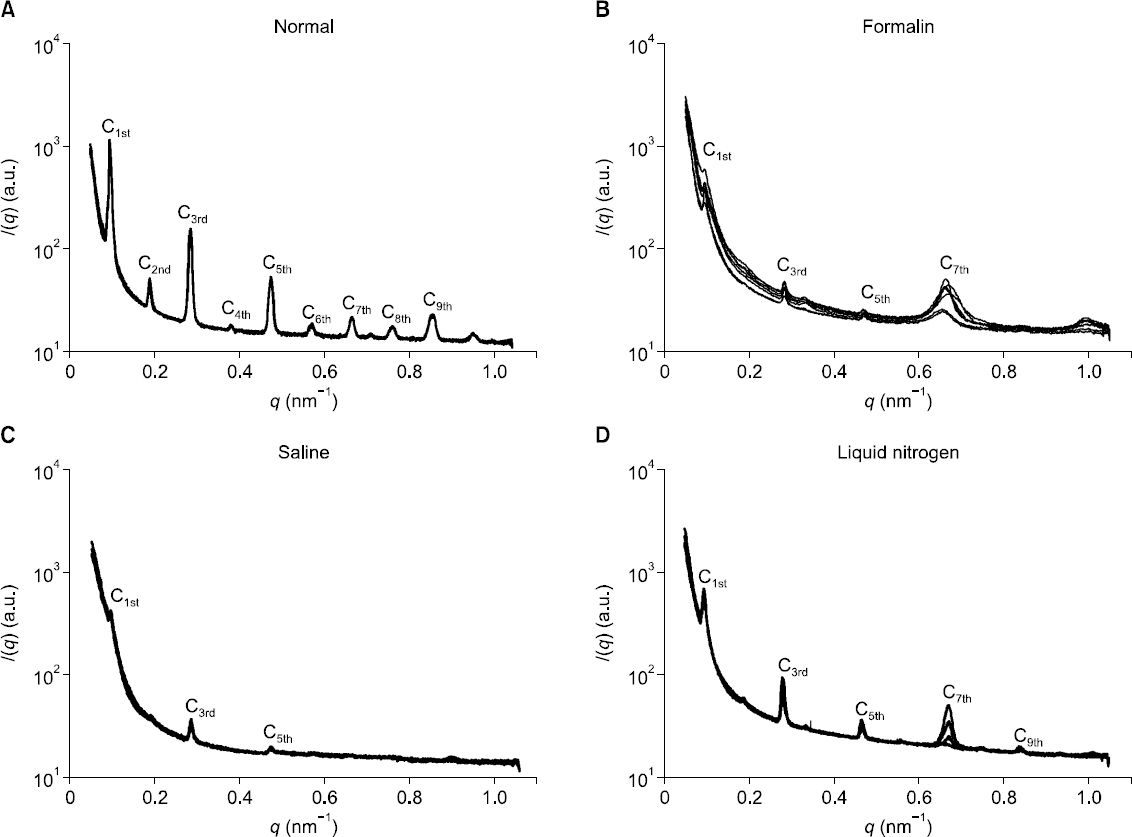
Fig.┬Ā2
One dimensional SAXS plot of nerve in ex vivo state (normal) and nerve preserved for one day in formalin, saline and liquid nitrogen (LN2) measured by using of SAXS at vertical direction. Collagen fiber was measured as 67 nm periodicity peak pattern (C1st-C9th) in ex vivo state (A). Periodic peaks, C1st-C9th, of the nerve preserved in formalin and saline were not measured and/or weak intensity (B, C). Periodic peaks and intensity, C1st-C9th, of the nerve preserved in liquid nitrogen were comparable to those of nerve in ex vivo state (D).
Ēżļź┤ļ¦Éļ”░(ņĢīļŹ░ĒĢśņØ┤ļō£Ļ│äņŚ┤ [0.1% Glutaaldehyde, GA + 4% Paraformaldehyde, PFA])ņØä ņé¼ņÜ®ĒĢśņŚ¼ ĻČüļæźņŗĀĻ▓Į ņĪ░ņ¦üņØä 1ņØ╝ ļÅÖņĢł ļ│┤ņĪ┤ĒĢ£ Ļ▓ĮņÜ░ņØś SAXS Ēī©Ēä┤
ņźÉ ĻČüļæźņŗĀĻ▓ĮņØä Ēżļź┤ļ¦Éļ”░ņŚÉ 1ņØ╝ ļÅÖņĢł ļ│┤ņĪ┤ĒĢśņŚ¼ ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ ņłśĒÅē ļ░®Ē¢źņŚÉņä£
Fig. 1BņÖĆ Ļ░ÖņØ┤ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī ņé¼ņØ┤ņØś Ļ▒░ļ”¼ļź╝ ļéśĒāĆļé┤ļŖö ĒÜīņĀł peakņØĖ F
1st, F
2ndĻ░Ć ņĖĪņĀĢļÉśņ¦Ć ņĢŖņĢśņ£╝ļ®░, ņłśņ┤łļź╝ ļéśĒāĆļé┤ļŖö M
1st, M
2nd ĻĘĖļ”¼Ļ│Ā M
3rdņØś ĒÜīņĀł peakĻ░Ć ņĖĪņĀĢņØĆ ļÉśņŚłņ£╝ļéś ņäĖĻĖ░Ļ░Ć ļ¦żņÜ░ ņĢĮĒ¢łļŗż. ņłśņ¦üļ░®Ē¢źņŚÉņä£ ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āļź╝ ļéśĒāĆļé┤ļŖö ĒÜīņĀł peak (C
1st-C
9th)ļÅä
Fig. 2B ņÖĆ Ļ░ÖņØ┤ ņŚŁņŗ£ ņäĖĻĖ░Ļ░Ć ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż.
ņāØļ”¼ņŗØņŚ╝ņłśņŚÉ ņŗĀĻ▓ĮņĪ░ņ¦üņØä 1ņØ╝ ļÅÖņĢł ļ│┤ņĪ┤ĒĢ£ ņźÉņØś ĻČüļæźņŗĀĻ▓ĮņØś SAXS Ēī©Ēä┤
ņźÉ ĻČüļæźņŗĀĻ▓ĮņØä ņāØļ”¼ņŗØņŚ╝ņłśņŚÉ ĒĢśļŻ© ļÅÖņĢł ļ│┤ņĪ┤ ĒĢ£ Ēøä ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ ņłśĒÅē ļ░®Ē¢źņŚÉņä£
Fig. 1CĻ│╝ Ļ░ÖņØ┤ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī Ļ░äņØś Ļ▒░ļ”¼ļź╝ ļéśĒāĆļé┤ļŖö ĒÜīņĀł peakņØĖ F
1st, F
2ndĻ░Ć ņĖĪņĀĢļÉśņ¦Ć ņĢŖņĢśĻ│Ā ņłśņ┤łņØś ĒÜīņĀł peakņØĖ M
1st, M
2nd ĻĘĖļ”¼Ļ│Ā M
3rdņØś ņØ╝ļČĆļČäņØ┤ ņĖĪņĀĢļÉśņ¦Ć ņĢŖņĢśĻ│Ā ņĖĪņĀĢļÉ£ peakņŚÉņä£ļÅä ĻĘĖ ņäĖĻĖ░ļŖö ļ¦żņÜ░ ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż. ĻĘĖļ”¼Ļ│Ā ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀļōżņØś ĒÜīņĀł peakņØĖ C
1st-C
9thņØś ņäĖĻĖ░ļÅä
Fig. 2CņŚÉņä£ņÖĆ Ļ░ÖņØ┤ ļ¦żņÜ░ ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż.
ņĢĪĒÖöņ¦łņåīņŚÉ ņŗĀĻ▓ĮņĪ░ņ¦üņØä 1ņØ╝ ļÅÖņĢł ļ│┤ņĪ┤ĒĢ£ ņźÉņØś ĻČüļæźņŗĀĻ▓ĮņØś SAXS Ēī©Ēä┤
ņźÉ ĻČüļæźņŗĀĻ▓ĮņØä ņĢĪĒÖöņ¦łņåīņŚÉ ĒĢśļŻ© ļÅÖņĢł ļ│┤Ļ┤ĆĒĢ£ Ēøä ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝
Fig. 1ņÖĆ
Fig. 2DņŚÉņä£ņÖĆ Ļ░ÖņØ┤ ņłśņ┤ł(M
1st, M
2nd ĻĘĖļ”¼Ļ│Ā M
3rd), ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī Ļ░äņØś Ļ▒░ļ”¼(F
1st, F
2nd) ĻĘĖļ”¼Ļ│Ā ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀļōżņØś ĒÜīņĀłĒö╝Ēü¼(C
1st-C
9th)ļŖö ex-vivo ņāüĒā£ ņĖĪņĀĢĒĢ£ Ļ▓ĮņÜ░ņÖĆ ņ£Āņé¼ĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłļŗż.
Ļ│Āņ░░
ņåīĻ░ü X-ņäĀ ņé░ļ×Ć ĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŗĀĻ▓Į ĻĄ¼ņĪ░ņØś ļ│ĆĒÖöļź╝ ņĖĪņĀĢĒĢĀ ņłś ņ׳ņ£╝ļéś[
2,
3] ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░Ļ░Ć ĻĄŁļé┤ņŚÉņä£ ĒżĒĢŁ ĒĢ£Ļ││ņŚÉļ¦ī ņ׳ĻĖ░ņŚÉ ņØ┤ļź╝ ņØ┤ņÜ®ĒĢśļŖö ņŗ£Ļ░äņŚÉ ņĀ£ĒĢ£ņØ┤ ņ׳ļŗż. ĻĘĖļ¤¼ļ»ĆļĪ£ ļ»Ėļ”¼ ņŗżĒŚśļ¬©ļŹĖņØä ļ¦īļōżĻ│Ā ņŗ£ļŻīļź╝ ņĀüņČ£ĒĢśņŚ¼ ļ│┤Ļ┤ĆĒĢ£ Ēøä Ļ░ĆņĀĖĻ░Ćņä£ ņŗżĒŚśņØä ĒĢśļ®┤ ņØ┤ļź╝ ņ¢┤ļŖÉ ņĀĢļÅä ļ│┤ņÖäĒĢĀ ņłśĻ░Ć ņ׳ļŗżĻ│Ā ņāØĻ░üļÉśĻĖ░ņŚÉ ņØ┤ņŚÉ ņ×äņāüņŚÉņä£ ņĪ░ņ¦üņØś ļ│┤Ļ┤ĆņØä ņ£äĒĢ┤ ņé¼ņÜ®ĒĢśļŖö Ēżļź┤ļ¦Éļ”░Ļ│╝ ņĢĪĒÖöņ¦łņåī, ĻĘĖļ”¼Ļ│Ā ņāØļ”¼ņŗØņŚ╝ņłśļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņŗĀĻ▓ĮņĪ░ņ¦üņØä ļ│┤Ļ┤ĆĒĢ£ Ēøä ņŗżĒŚśņØä ņŗ£Ē¢ēĒĢĀ ņŗ£ ņØ┤ļōż ļ│┤ņĪ┤ļ░®ļ▓ĢņØ┤ SAXSņØś Ļ▓░Ļ│╝ņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØ┤ ņ׳ļŖöĻ░Ćļź╝ ņĪ░ņé¼ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ņ¢┤ ĒżĒĢŁ Ļ░ĆņåŹĻĖ░ 4C1 SAXS 1 ļ╣ö ļØ╝ņØĖņŚÉņä£ ļ│Ė ņŗżĒŚśņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ĻĘĖ Ļ▓░Ļ│╝ ņĢĪĒÖöņ¦łņåīņŚÉ ļ│┤Ļ┤Ć ĒĢ£ Ļ▓ĮņÜ░ņŚÉļŖö ņŗżĒŚśņ¦üņĀäņŚÉ ņĪ░ņ¦üņØä ņĀüņČ£ĒĢ£ ex vivoņāüĒā£ņŚÉņä£ SAXSĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ņÖĆ ļ╣äĻĄÉ ņŗ£ ņ£Āņé¼ĒĢśņśĆņ£╝ļéś Ēżļź┤ļ¦Éļ”░Ļ│╝ ņāØļ”¼ņŗØņŚ╝ņłśņŚÉ ļ│┤Ļ┤ĆĒĢśļŖö ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢ£ Ļ▓ĮņÜ░ņŚÉņä£ļŖö SAXS Ēī©Ēä┤ņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ļīĆņĪ░ĻĄ░ņØĆ SAXSļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŗżĒŚśĒĢśĻĖ░ ņ¦üņĀäņŚÉ ĻČüļæźņŗĀĻ▓ĮņØä ņĀüņČ£ĒĢśņśĆļŗż. ņŗĀĻ▓ĮņØä ņłśņ¦üņ£╝ļĪ£ Ļ▒░ņ╣śĒĢ£ Ēøä SXASĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņłśĒÅēļ░®Ē¢źņ£╝ļĪ£ ņĖĪņĀĢĒĢśļ®┤ ņłśņ┤łņÖĆ ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņåīĻ░äņØś Ļ▒░ļ”¼ļź╝ ļéśĒāĆļé┤ļŖö ĒÜīņĀł Ēö╝Ēü¼ Ēī©Ēä┤ņØä ņĖĪņĀĢĒĢĀ ņłś ņ׳ņ£╝ļ®░ ņłśņ¦üļ░®Ē¢źņ£╝ļĪ£ ņĖĪņĀĢĒĢśļ®┤ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āļź╝ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŗż. ņłśĒÅēļ░®Ē¢źņŚÉņä£ ņĖĪņĀĢ ņŗ£ 18 nmņØś ņŻ╝ĻĖ░ņä▒ņØä ļéśĒāĆļé┤ļŖö ĒÜīņĀł Ēö╝Ēü¼Ļ░Ć ņĖĪņĀĢļÉśņŚłļŖöļŹ░ ņØ┤ļ¤¼ĒĢ£ ĒÜīņĀł Ēö╝Ēü¼ļōżņØĆ ņłśņ┤łņØś ņØ┤ņżæ ļ¦ē(double membrane) ĻĄ¼ņĪ░ņŚÉ ĻĖ░ņØĖĒĢ£ļŗż[
6]. ņłśņ┤łļŖö 40%ņØś ņłśļČä, ņ¦Ćņ¦ł(42-51%), ļŗ©ļ░▒ņ¦ł(9-18%) ņä▒ļČäņ£╝ļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņ׳ļŖöļŹ░, ļŗ©ļ░▒ņ¦łņØĆ ņČĢņāēļÅīĻĖ░ ņŻ╝ņ£äļź╝ ļÅÖņŗ¼ņøÉņ£╝ļĪ£ Ļ░ÉņŗĖĻ│Ā ņ׳ļŖö ņ¢ćņØĆ ĒīÉņ£╝ļĪ£ ņĪ┤ņ×¼ĒĢśĻ│Ā ņ¦Ćņ¦łņØś ņØ┤ļČäņ×É ņĖĄļōż(two bimolecular layers)ņØĆ ņØ┤ņøāĒĢ£ ļŗ©ļ░▒ņ¦ł ņĖĄļōż ņé¼ņØ┤ņŚÉ ļü╝ņ¢┤ ļōżņ¢┤Ļ░Ć ņ׳ļŖö ĒŖ╣ņØ┤ĒĢ£ ĻĄ¼ņĪ░ņØ┤ļŗż. ļśÉĒĢ£ ĒÅŁņØ┤ ņāüļŗ╣Ē׳ ļäōĻ│Ā ĒÜīņĀłņäĖĻĖ░Ļ░Ć ņĢĮĒĢ£ 66 nmņØś ņŻ╝ĻĖ░ņä▒ņØä ļéśĒāĆļé┤ļŖö ĒÜīņĀł Ēö╝Ēü¼Ļ░Ć ņĖĪņĀĢļÉśņŚłļŖöļŹ░[
7] ņØ┤ļ¤¼ĒĢ£ peakļōżņØĆ ņłśņ¦üņ£╝ļĪ£ ņ£äņ╣śĒĢ£ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī ņé¼ņØ┤ņØś Ļ░äĻ▓®(interfibrillar space)ņØä ļéśĒāĆļé┤ļŖö Ļ▓āņØ┤ļŗż. ĻĘĖļ”¼Ļ│Ā ņłśņ¦üļ░®Ē¢źņ£╝ļĪ£ ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ ņłśĒÅēļ░®Ē¢źĻ│╝ ļ╣äņŖĘĒĢśĻ▓ī ņĢĮ 67 nm ņØś ņŻ╝ĻĖ░ņä▒ņØä Ļ░Ćņ¦ĆļŖö ĒÜīņĀłĒī©Ēä┤ņØä ļ│┤ņØ┤Ļ│Ā ņ׳ņØīņØ┤ ņĖĪņĀĢļÉśņŚłļŖöļŹ░ ņØ┤ļŖö ņŗĀĻ▓Į ļ¦ēņØä ņØ┤ļŻ©Ļ│Ā ņ׳ļŖö ņŻ╝ņä▒ļČäņØĖ ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņØś ĻĘ£ņ╣ÖņĀüņØĖ ĻĄ¼ņĪ░ļź╝ ļéśĒāĆļé┤ļŖö Ļ▓āņØ┤ļŗż[
8]. ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀļŖö ļ¦Éļŗ©ņØ┤ Ļ░üĻ░ü Ēāäņåī(C-terminal)ņÖĆ ņ¦łņåī(N-terminal)ļĪ£ ļüØļéśļŖö ĻĖĖņØ┤ ņĢĮ 300 nm ņĀĢļÅäņØś ņĮ£ļØ╝Ļ▓É ļ¦łņØ┤Ēü¼ļĪ£ ņä¼ņ£Ā ļŗżļ░£ņØ┤ ļŁēņ│ÉņĀĖņä£ ĒśĢņä▒ļÉśļŖöļŹ░[
9] ņØ┤ļōżņØ┤ ļŗżļ░£ļĪ£ ļŁēņ│Éņ¦ł ļĢī, Ļ░ü ļ¦Éļŗ©ņØ┤ ņä£ļĪ£ ņ¦üņĀæ ņŚ░Ļ▓░ļÉśņ¦Ć ņĢŖĻ│Ā Ēŗłņāłļź╝ Ļ░Ćņ¦ĆĻ▓ī ļÉśņ¢┤ ņżæņ▓® ņśüņŚŁ(ņĀäņ×Éļ░ĆļÅäĻ░Ć ļåÆņØĆ ņśüņŚŁ)Ļ│╝ Ļ░Ł ņśüņŚŁ(ņĀäņ×Éļ░ĆļÅäĻ░Ć ļé«ņØĆ ņśüņŚŁ)ņØ┤ ļ░śļ│ĄņĀüņØ┤Ļ│Ā ĻĘ£ņ╣ÖņĀüņØĖ ĒŖ╣ņØ┤ĒĢ£ ĻĄ¼ņĪ░ļź╝ ĒśĢņä▒ĒĢśĻ▓ī ļÉ£ļŗż. ņØ┤ ņśüņŚŁņØś ļŗ©ņ£ä ĻĖĖņØ┤(ņżæņ▓®ņśüņŚŁ + Ļ░Ł ņśüņŚŁ)Ļ░Ć ņČĢ ņŻ╝ĻĖ░ņä▒ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö 67 nm ņØ┤ļŗż. ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņØś ĒÜīņĀł Ēö╝Ēü¼ļōż ņżæņŚÉņä£
Fig. 2AņŚÉņä£ņÖĆ Ļ░ÖņØ┤ ĒŖ╣Ē׳ ĒÖĆņłś ņ░©ņłś ĒÜīņĀł Ēö╝Ēü¼ļōżņØ┤ ļ¦żņÜ░ Ļ░ĢĒĢ£ ņäĖĻĖ░Ļ░Ć ņĖĪņĀĢļÉśņŚłļŗż. ņØ┤Ļ▓āņØĆ ĒÜīņĀł Ēö╝Ēü¼ ņé¼ņØ┤ņØś Ļ░Ł ņśüņŚŁņØ┤ ļ»Ėļäżļ×ä ļō▒ņ£╝ļĪ£ ņ▒äņøīņ¦Ćņ¦Ć ņĢŖĻ│Ā ļ╣äņ¢┤ņ׳ņØīņØä ņĢöņŗ£ĒĢ£ļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ ļ╝ł ļō▒Ļ│╝ Ļ░ÖņØĆ ņ¦Ćņ¦Ć ĻĄ¼ņĪ░ņ▓┤ ņĪ░ņ¦üņØś Ļ▓ĮņÜ░ņŚÉļŖö Ļ░Ł ņśüņŚŁņØĆ ļ¼┤ĻĖ░ņ¦ł ļ»Ėļäżļ×ä ņä▒ļČäņ£╝ļĪ£ ņ▒äņøīņ¦Ćļ®░ ņØ┤ļĢīļŖö ņ¦Øņłś ņ░©ņłśņØś ĒÜīņĀłĒö╝Ēü¼ļōżņØś ņāüļŗ╣ĒĢ£ ņäĖĻĖ░Ļ░Ć ļéśĒāĆļé£ļŗż[
10].
ņŗżĒŚś ĻĄ░ņŚÉņä£ ņźÉ ĻČüļæźņŗĀĻ▓ĮņØä ņĀüņČ£ Ēøä ņĢīļŹ░ĒĢśņØ┤ļō£Ļ│äņŚ┤ (0.1% GA + 4% PFA, Ēżļź┤ļ¦Éļ”░)ņØä ņé¼ņÜ®ĒĢśņŚ¼ ņŗĀĻ▓ĮņĪ░ņ¦üņØä 1ņØ╝ ļÅÖņĢł ļ│┤ņĪ┤ĒĢ£ Ēøä SAXSĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢśņśĆļŗż. Ļ┤æĒĢÖĒśäļ»ĖĻ▓ĮņØ┤ļéś ņĀäņ×ÉĒśäļ»ĖĻ▓ĮņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŚ░ĻĄ¼ĒĢĀ ņŗ£ņŚÉļŖö ņĪ░ņ¦üņØś Ļ│ĀņĀĢņĢĪņ£╝ļĪ£ ņĢīļŹ░ĒĢśņØ┤ļō£Ļ│äņÖĆ ĻĖłņåŹņŚ╝ Ļ│ĀņĀĢņĢĪ(ņśżņŖżļŖä)ņØ┤ ņé¼ņÜ®ļÉ£ļŗż. ĒŖ╣Ē׳ ņĢīļŹ░ĒĢśņØ┤ļō£Ļ│äņŚ┤ņØś ņÜ®ņĢĪņØĆ Ēśäļ»ĖĻ▓ĮņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĪ░ņ¦üņØä Ļ▓Ćņé¼ĒĢĀ ņŗ£ņŚÉ ņĪ░ņ¦üĻ│ĀņĀĢņØä ņ£äĒĢśņŚ¼ ļäÉļ”¼ ņé¼ņÜ®ļÉśņ¢┤ ņ¦ĆĻ│Āņ׳ļŗż. ņØ┤ ņÜ®ņĢĪņØä ņé¼ņÜ®ĒĢĀ ņŗ£ņŚÉļŖö ņäĖĒżņØś ņä▒ļČä ņżæ ļŗ©ļ░▒ ņØæĻ│ĀņÖĆ ņ╣©ņĀä, ņĪ░ņ¦üņØś Ļ▓ĮĒÖöļź╝ ņ£Āļ░£ņŗ£ņ╝£ ņĪ░ņ¦üņØś ņ×ÉĻ░Ćņ£ĄĒĢ┤ļź╝ ļ░®ņ¦ĆĒĢśņŚ¼ ņāØņ▒äņÖĆ Ļ░ĆĻ╣ØĻ▓ī ļ¦īļōż ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ņĢīļŹ░ĒĢśņØ┤ļō£Ļ│ä ņóģļźśņØś Ļ│ĀņĀĢņĢĪņ£╝ļĪ£ļŖö ĻĖĆļŻ©ĒāĆņĢīļŹ░ĒĢśņØ┤ļō£(Glutaaldehyde, GA) ņÖĆ ĒīīļØ╝Ēżļ”äņĢīļŹ░ĒĢśņØ┤ļō£(Paraformaldehyde, PFA)Ļ░Ć ĒØöĒ׳ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż. GAļź╝ ņé¼ņÜ®ĒĢĀ ņŗ£ņŚÉļŖö ņØ┤ ņÜ®ņĢĪņØ┤ ļČłņĢłņĀĢĒĢśņŚ¼ ņé░(acid)ņØä ļ¦īļōżĻĖ░ ņēĮĻ│Ā, ļČłņł£ļ¼╝ņØ┤ ņä×ņØ╝ ņłśĻ░Ć ņ׳ņ¢┤ ĒÆłņ¦łņØ┤ ņĀĆĒĢśļÉśĻ│Ā Ļ│ĀņĀĢņ×æņÜ®ņØ┤ ļ¢©ņ¢┤ņ¦ĆļŖö ļŗ©ņĀÉņØ┤ ņ׳ĻĖ░ņŚÉ PFAņÖĆ Ēś╝ĒĢ®ĒĢśņŚ¼ ņé¼ņÜ®ĒĢ£ļŗż. PFAņÖĆ Ēś╝ĒĢ®ĒĢśņŚ¼ ņé¼ņÜ®ņŗ£ ļŗ©ļ░▒ņ¦ł ņ╣©ņĀäņ×æņÜ®ņØ┤ ņ׳ņ¢┤ ļŗ©ļ░▒ņ¦ł ļ│┤ņĪ┤ĒÜ©Ļ│╝Ļ░Ć ņÜ░ņłśĒĢśļŗż. ĒŖ╣Ē׳ ņĀäņ×ÉĒśäļ»ĖĻ▓ĮņØä ņØ┤ņÜ®ĒĢĀ Ļ▓ĮņÜ░ ņäĖĒżļ¦ē Ļ│äņØś ļ│┤ņĪ┤ņØ┤ ņóŗĻ│Ā, ļ»ĖņäĖĻ┤Ć, ņĢäĻĄÉņ¦łņä¼ņ£Ā, ĒāäļĀźņä¼ņ£Ā ļō▒ņØ┤ ņäĀļ¬ģĒĢśĻ▓ī ļ│┤ņØ┤ļŖö ņןņĀÉņØ┤ ņ׳ļŗż. ĻĘĖļ¤¼ļéś Ļ│ĀņĀĢņĢĪņØś ņ╣©Ēł¼Ļ░Ć ļéśņüśļ®░, ņĪ░ņ¦üņØ┤ ļČĆņä£ņ¦ĆĻĖ░ ņēĮĻ│Ā, ļ░ĢņĀłĒĢśĻĖ░ Ļ│żļ×ĆĒĢśļŗżļŖö ļŗ©ņĀÉļÅä ņ׳ļŗż[
11]. Changizi ļō▒[
12]ņŚÉ ņØśĒĢśļ®┤ ņ£Āļ░®ņĢöņĪ░ņ¦üņØä Ēżļź┤ļ¦Éļ”░ņŚÉ ļ│┤ņĪ┤ĒĢśņŚ¼ SAXSĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢśļŖö ļ░®ļ▓ĢņØĆ ņĪ░ņ¦üļ│æļ”¼ĒĢÖņĀüņØĖ ņłśĻĖ░ļĪ£ ļČĆņĀüņĀłĒĢśļŗżĻ│Ā ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņāüņŚÉņä£ļŖö 0.1% GA + 4% PFAļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ļ│┤ņĪ┤ĒĢśņŚ¼ SAXSĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĖĪņĀĢĒĢ£ Ļ▓░Ļ│╝ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī ņé¼ņØś Ļ▒░ļ”¼ļź╝ ļéśĒāĆļé┤ļŖö ĒÜīņĀł peakņØĖ F
1st, F
2ndĻ░Ć ņĖĪņĀĢļÉśņ¦Ć ņĢŖņĢśņ£╝ļ®░, ņłśņ┤łļź╝ ļéśĒāĆļé┤ļŖö M
1st, M
2nd ĻĘĖļ”¼Ļ│Ā M
3rdņØś ĒÜīņĀł peakĻ░Ć ņĖĪņĀĢņØĆ ļÉśņŚłņ£╝ļéś ņäĖĻĖ░Ļ░Ć ļ¦żņÜ░ ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłĻ│Ā ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņØś ĒÜīņĀł peakļÅä ņŚŁņŗ£ ņäĖĻĖ░Ļ░Ć ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśļŖö ļō▒ ņłśņ┤łņØś ņåÉņāüĻ│╝ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī ņé¼ņØ┤ņØś Ļ▒░ļ”¼ņØś ņåÉņāü ĻĘĖļ”¼Ļ│Ā ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņåīļÅä ņŚŁņŗ£ ņåÉņāüļÉ£ Ļ▓āņ£╝ļĪ£ ņĖĪņĀĢļÉśņŚłļŖöļŹ░ ņØ┤ļ¤¼ĒĢ£ Ļ▓░Ļ│╝ļŖö ņŗĀĻ▓ĮņĪ░ņ¦üņŚÉ ņ׳ļŖö ļŗ©ļ░▒ņ¦łņØś ļ│ĆĒÖöļź╝ ņĢ╝ĻĖ░ņŗ£ņ╝░ĻĖ░ ļĢīļ¼ĖņØ┤ļØ╝Ļ│Ā ņāØĻ░üļÉ£ļŗż.
ņāØļ”¼ņŗØņŚ╝ņłśļĪ£ ņĪ░ņ¦ü ļ│┤ņĪ┤ĒĢśļŖö ļ░®ļ▓ĢņØĆ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ¦ĆļŖö ņĢŖņ£╝ļéś Ļ░Ćļüö ĒāĆ ļ│┤ņĪ┤ ņĢĪņ£╝ļĪ£ Ēś╝ļÅÖĒĢśņŚ¼ ņé¼ņÜ®ĒĢĀ ņłśĻ░Ć ņ׳ņ¢┤ ņØ┤ņØś ņĀüņĀĢņä▒ņØä ĒÅēĻ░ĆĒĢśņśĆļŗż. ņāØļ”¼ņŗØņŚ╝ņłśņŚÉ ļ│┤ņĪ┤ĒĢ£ Ļ▓ĮņÜ░ ņłśĒÅēļ░®Ē¢źĻ│╝ ņłśņ¦ü ļ░®Ē¢źņŚÉņä£ ņĖĪņĀĢļÉśļŖö ņłśņ┤ł, ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī Ļ░äņØś Ļ▒░ļ”¼ ĻĘĖļ”¼Ļ│Ā ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī ļōżņØä ņĖĪņĀĢĒĢ£ SAXS Ļ▓░Ļ│╝ ņĮ£ļØ╝Ļ▓É ņä¼ņ£Āņåī Ļ░äņØś Ļ▒░ļ”¼ļź╝ ļéśĒāĆļé┤ļŖö ĒÜīņĀł peakļŖö ņĖĪņĀĢļÉśņ¦Ć ņĢŖņĢśĻ│Ā, ņłśņ┤łļź╝ ļéśĒāĆļé┤ļŖö ĒÜīņĀł peakņØś ņäĖĻĖ░ ļśÉĒĢ£ ļ¦żņÜ░ ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśņŚłņ£╝ļ®░ ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀņØś ĒÜīņĀł peakņØś ņäĖĻĖ░ļōżļÅä ļ¦żņÜ░ ņĢĮĒĢśĻ▓ī ņĖĪņĀĢļÉśļŖö ļō▒ ļ¦ÄņØĆ ņåÉņāüņØ┤ ļ░£ņāØĒĢśņŚ¼ Ēżļź┤ļ¦Éļ”░ ļ│┤ņĪ┤ ņŗ£ņÖĆ Ļ░ÖņØ┤ SAXSļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņŚ░ĻĄ¼ ņŗ£ ņĪ░ņ¦üņØś ļ│┤ņĪ┤ ļ░®ļ▓ĢņØ┤ ņĀüņĀłĒĢśņ¦Ć ļ¬╗ĒĢśļŗżļŖö Ļ▓░ļĪĀņØä ņ¢╗ņŚłļŗż. ņØ┤ļ¤¼ĒĢ£ ņøÉņØĖņØĆ ņāØļ”¼ņŗØņŚ╝ņłśņŚÉ ņØśĒĢ£ ņé╝Ēł¼ņĢĢņŚÉ ņØśĒĢ£ ņĪ░ņ¦üņåÉņāüņŚÉ ņØśĒĢ£ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ņĢĪĒÖöņ¦łņåīņŚÉ ļ│┤ņĪ┤ĒĢ£ ĻĄ░ņŚÉņä£ļŖö ņĢĪĒÖöņ¦łņåīņŚÉ ļ│┤ņĪ┤ĒĢśņŚ¼ ĒĢśļŻ©ļź╝ ņ¦Ćļé£ ĒøäņŚÉ ņĖĪņĀĢĒĢśņśĆļŗż. ņĢĪĒÖöņ¦łņåīņŚÉ ļ│┤ņĪ┤ĒĢśļŖö ļ░®ļ▓ĢņØĆ ņĪ░ņ¦üņØś ņøÉĒśĢņØä ņé┤ļ”¼ļ®┤ņä£ ĻĖēļāēĒĢśļŖö ļ░®ļ▓ĢņØ┤ļŗż. ņØ┤ ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢĀ ņŗ£ņŚÉļŖö ņĪ░ņ¦üņØś ņżĆļ╣äĻ│╝ņĀĢņØ┤ ņŚåņØ┤ ņŗżĒŚśĒĢĀ ņłśĻ░Ć ņ׳ļŗż. ĻĘĖļ”¼Ļ│Ā Ēü░ ņś©ļÅä ļ│ĆĒÖö ņŚåņØ┤ ņØ╝ņĀĢ ņś©ļÅäļź╝ ņ£Āņ¦Ć ĒĢĀ ņłś ņ׳ļŖö ņןņĀÉņØ┤ ņ׳ļŗż. ļśÉĒĢ£ ņĀĆņןņś©ļÅäĻ░Ć ņäĖĒżĒÖ£ņä▒ĒÖöļź╝ ņ£Āņ¦ĆĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ņśüĒĢś 150ļÅäļź╝ ņ£Āņ¦ĆĒĢśņŚ¼ņĢ╝ ĒĢśļŖöļŹ░ ņĢĪņ▓┤ņ¦łņåīņŚÉ ļŗ┤Ļ▓©ņ׳ļŖö ņŗ£ļŻīņØś ņś©ļÅäļŖö ņśüĒĢś 196ļÅä ņØ┤ĻĖ░ņŚÉ ņäĖĒżņØś ļ│Ćņä▒ņØ┤ ņ£Āļ░£ļÉśņ¦Ć ņĢŖļŖöļŗż[
13]. Changizi ļō▒ņŚÉ[
14] ņØśĒĢśļ®┤ ņ£Āļ░®ņĢö ņĪ░ņ¦üņØä ņĢĪĒÖöņ¦łņåīļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņĪ░ņ¦üņØä ļ│┤ņĪ┤ĒĢśņŚ¼ Ļ▓░Ļ│╝ļź╝ ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░ ņØ┤ ļ░®ļ▓ĢņØ┤ ņĀüņĀłĒĢśļŗżĻ│Ā ĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņāüņŚÉņä£ļÅä ņłśņ¦üĻ│╝ ņłśĒÅēļ░®Ē¢źņŚÉņä£ ņĖĪņĀĢļÉ£ ņłśņ┤ł, ņä¼ņ£Āņåī Ļ░äņØś Ļ▒░ļ”¼ ĻĘĖļ”¼Ļ│Ā ņĮ£ļØ╝Ļ▓É ņä¼ņ£ĀļōżņØä ļéśĒāĆļé┤ļŖö ĒÜīņĀł Ēö╝Ēü¼ņÖĆ ņäĖĻĖ░Ļ░Ć ļ░®ņé¼Ļ┤æ Ļ░ĆņåŹĻĖ░ļĪ£ ņĖĪņĀĢĒĢśĻĖ░ ņ¦üņĀäņŚÉ ņĪ░ņ¦üņØä ņĀüņČ£ĒĢśņŚ¼ ex-vivo ņāüĒā£ļĪ£ ņĖĪņĀĢĒĢ£ Ļ▓ĮņÜ░ņÖĆ ļ╣äĻĄÉ ņŗ£ ņ£Āņé¼ĒĢ£ Ļ▓░Ļ│╝Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż. ĻĘĖļ¤¼ļ»ĆļĪ£ SAXSĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŚ░ĻĄ¼ĒĢĀ ņŗ£ņŚÉ ņ░©ņäĀņØś ļ░®ļ▓ĢņØ┤ļØ╝Ļ│Ā ņāØĻ░üļÉ£ļŗż.
ņłśņ┤łļŖö ņŖżļ®ĢĒŗ▒(Ļ░ĆļŖśĻ│Ā ĻĖ┤ ļČäņ×ÉĻ░Ć ĻĘĖ ņןņČĢņØä ņØ╝ņĀĢ ļ░®Ē¢źņ£╝ļĪ£ Ē¢źĒĢ┤ ņżä ņä£Ļ│Ā, ņśåņżä ļČäņ×ÉņÖĆ ņØ┤ņØīļ¦żĻ░Ć ņä£ļĪ£ ņØ╝ņ╣śĒĢśļŖö ņāüĒā£)ņØś ņĢĪņĀĢņä▒ ņāüĒā£ļź╝(fluid-crystalline or liquid-crystalline nature) Ļ░Ćņ¦äļŗż[
6]. ĻĘĖļ¤¼ļ»ĆļĪ£ ļīĆļČĆļČäņØś ņŗĀĻ▓ĮņØĆ ņŗżņś©ņŚÉņä£ ņĢĪņĀĢņāüĒā£ņØ┤ļ»ĆļĪ£ ļ¼╝ļ”¼ņĀü, ĒÖöĒĢÖņĀü ņŗ£ļŻī ņżĆļ╣äĻ│╝ņĀĢņŚÉ ņØśĒĢ┤ ĻĄ¼ņĪ░Ļ░Ć ļ│ĆĒśĢļÉśĻĖ░ļÅä ĒĢ£ļŗż[
15]. ĻĘĖļ¤¼ļ»ĆļĪ£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĀüņČ£ĒĢ£ ĻČüļæźņŗĀĻ▓ĮņØä ĒÅ┤ļ”¼ņØ┤ļ»Ėļō£ ĒĢäļ”ä ņé¼ņØ┤ņŚÉ ļü╝ņøī ļäŻņØĆ Ēøä ņל ļ░Ćļ┤ēĒĢśņŚ¼ ņĖĪņĀĢĒĢśļŖö ļÅÖņĢł ņłśļČäņØś ņ”Øļ░£ņŚÉ ņØśĒĢ£ ļ│ĆĒśĢņØä ļ░®ņ¦ĆĒĢśņśĆļŗż.
Ļ▓░ļĪĀņĀüņ£╝ļĪ£ ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ Ēżļź┤ļ¦Éļ”░Ļ│╝ ņāØļ”¼ņŗØņŚ╝ņłśņŚÉ Ļ│ĀņĀĢĒĢśļŖö ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢ£ Ļ▓ĮņÜ░ņŚÉņä£ļŖö SAXS Ēī©Ēä┤ņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö Ļ▓āņ£╝ļĪ£ ņĖĪņĀĢļÉśņŚłĻĖ░ņŚÉ ņØ┤ļ¤¼ĒĢ£ ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢśļŖö Ļ▓āņØ┤ ļČĆņĀüņĀłĒĢśļŗżĻ│Ā ĒīÉļŗ©ļÉ£ļŗż. ĻĘĖļ¤¼ļéś ņĢĪĒÖöņ¦łņåīņŚÉ ļ│┤Ļ┤Ć Ē¢łļŹś Ļ▓ĮņÜ░ņŚÉņä£ļŖö ņŗżĒŚśņ¦üņĀäņŚÉ ņĪ░ņ¦üņØä ņĀüņČ£ĒĢśņŚ¼ ex vivoņāüĒā£ņŚÉņä£ ņĖĪņĀĢĒĢ£ SAXS Ļ▓░Ļ│╝ņÖĆ ņ£Āņé¼ĒĢśļŗżĻ│Ā ĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ¤¼ļ»ĆļĪ£ SAXSĻĖ░ļ▓ĢņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŗĀĻ▓ĮņĪ░ņ¦üņØä ņĖĪņĀĢĒĢśĻ│Āņ×É ĒĢĀ ņŗ£ņŚÉļŖö ņĖĪņĀĢņ¦üņĀäņŚÉ ņŗĀĻ▓ĮņĪ░ņ¦üņØä ņĀüņČ£ Ēś╣ņØĆ ļģĖņČ£ĒĢśņŚ¼ ņøÉĒśĢ ĻĘĖļīĆļĪ£ļź╝ ņØ┤ņÜ®ĒĢśļŖö Ļ▓āņØ┤ ļ░öļ×īņ¦üĒĢśļéś ņĢĪĒÖöņ¦łņåīņŚÉ ļ│┤Ļ┤ĆĒĢ£ Ēøä ņĖĪņĀĢĒĢśņŚ¼ļÅä ļ¼┤ļ░®ĒĢśļŗżĻ│Ā ņāØĻ░üļÉ£ļŗż.






